水光针埋线热玛吉纳入最高类医械管理引发关注
发布时间: 2022-04-08 16:09:28 | 来源: 中国网健康 | 责任编辑: 张丰
3月30日,国家药品监督管理局经过将近半年广泛征集调整意见,出台了《医疗器械分类目录》部分医疗器械调整内容的公告。

据悉,本次调整是为进一步深化医疗器械审评审批制度改革,依据医疗器械产业发展和监管工作实际,按照《医疗器械监督管理条例》、《医疗器械分类目录动态调整工作程序》的有关要求,对27类医疗器械内容进行调整,其中包括射频治疗(非消融)设备、整形美容用注射材料、整形用植入线材等产品类别。
我国对于医疗器械有着严格的分类,而三类医疗器械是最高级别的医疗器械。也就是说,目前大家常见的面部埋线项目,以玻尿酸、水光针等为代表的注射用透明质酸钠溶液,以热玛吉、热提拉、黄金微针为代表的射频治疗仪,均与人工心脏瓣膜、人工关节、血管支架等一样,同属于植入人体、对人体具有潜在危险,对其安全性、有效性必须严格控制的医疗器械。
调整公告公示后,立即引起社会广泛关注,尤其涉及整形的产品全部被纳入第三类管理类别,更是引起医疗美容行业的强烈反响。许多整形行业内的专家认为,这意味着处于行业上游的医疗器械领域正呈现加强监管的态势,具体来看有三种变化:
第一,从无到最严。本次调整中,面部埋植线、面部提拉线在调整前是没有被列入《医疗器械分类目录》中,调整后直接被列入最高类。
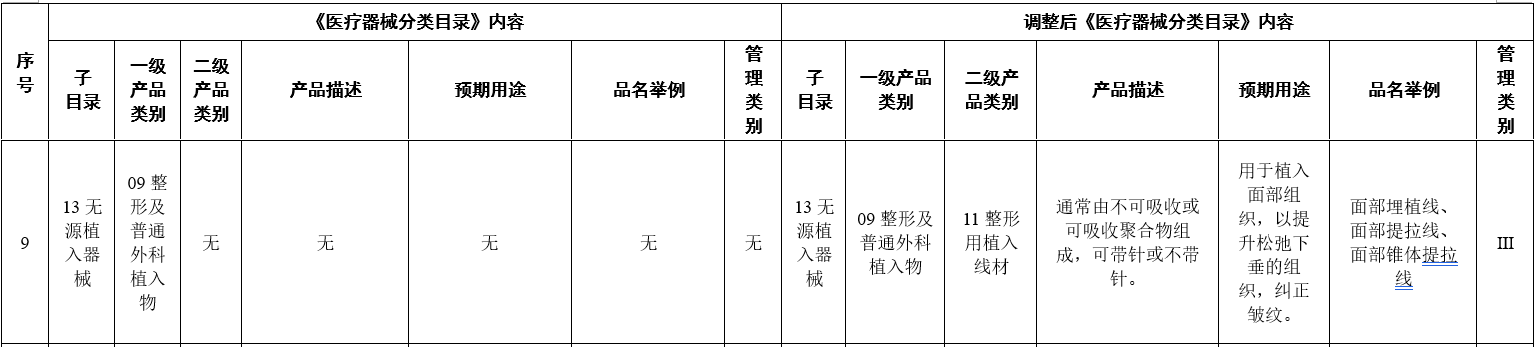
第二,从二类到三类。此次调整对风光无限的热玛吉,特别是争议不断的热玛吉五代做了界定。事实上,在2021年4月24日,国家药品监督管理局就发布了关于征求《射频美容类产品分类界定指导原则》(征求意见稿),对于热玛吉五代的射频美容类产品进行了界定。
射频医美项目的应用领域主要为抗衰老,属于微创治疗。治疗前需要局部麻醉,手术过程中有痛感,术后面部会出现红肿或少量结痂。截至2021年10月,通过国家药品监督管理局认证的有21款,国内自主研发的射频医美器械仅有武汉中科科里和德技医疗器械的2款器械。
值得注意的是,在去年11月公布的征求意见稿中,将用于面部、体部、颈部等非创伤性浅表治疗的高频电场皮肤热治疗仪、射频治疗仪,拟按照II类器械监管。正式调整后,均为第三类。
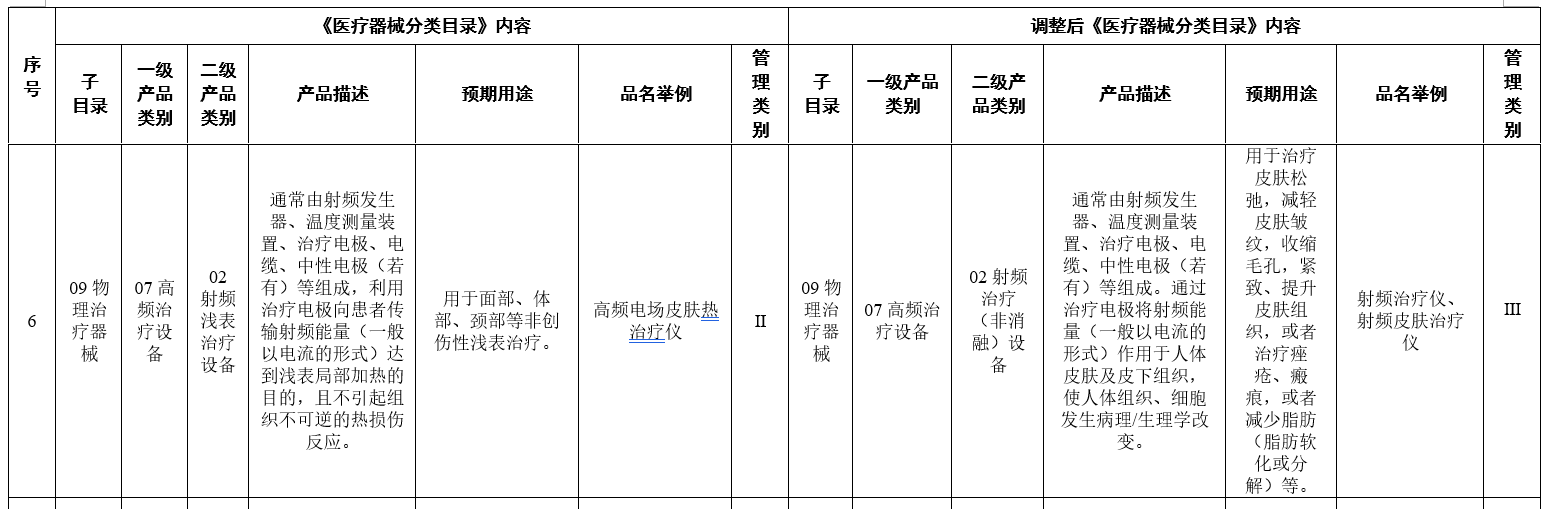
另外,留给射频器械生产厂商、销售商只有两年的调整时间,2024年4月1日后,未取得医疗器械注册证不得生产、进口和销售。
第三,调整前就属于三类器械的整形用注射填充物虽然级别不变,但是在产品描述、预期用途、品名举例中,都做了内容调整。《目录》显示,注射用透明质酸钠溶液,用于注射到真皮层,主要通过所含透明质酸钠等材料的保湿、补水等作用,改善皮肤状态,明确按照III类医疗器械监管。
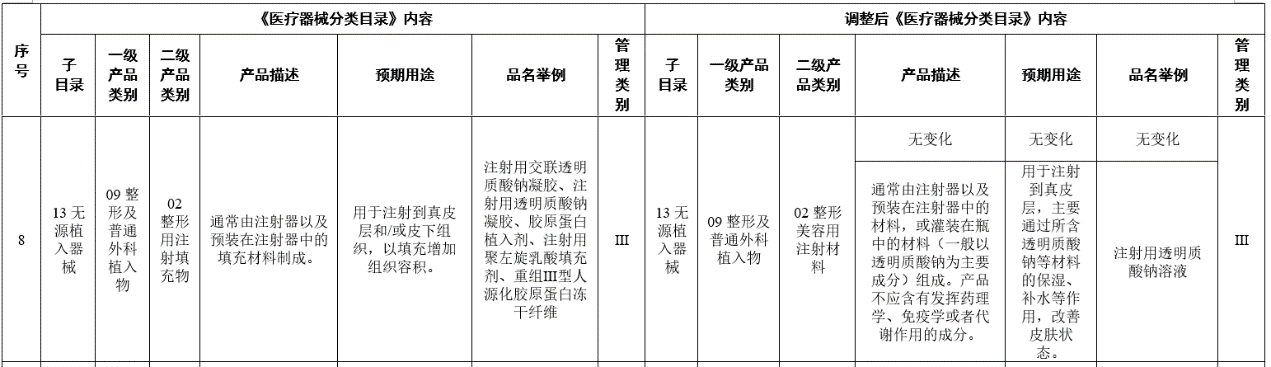
由此可以看出,此次调整对医美器械管理赋予了积极意义,特别是针对无证照的非法黑医美打击力度更大。其一,说明皮肤修复、面部抗衰等医美的网红项目,相关诊疗办法和医疗器械应用也逐渐成熟,以后不能再打擦边球;其二,明确医疗属性,明确射频治疗仪、面部埋植线及提拉线、注射用透明质酸钠溶液属于具有较高风险,需要采取特别措施严格控制管理以保证其安全、有效的医疗器械;其三,医美行业上游厂商纳入强监管,完善医美全产业链监管范围,为消费者提供全方位的安全保障。
值得注意的是,国家药品监督管理局在公布《医疗器械分类目录》部分医疗器械内容的同一天,还刊登了全国市场监管部门广告监管工作会议的报道。

会议以视频形式召开,全面总结2021年广告监管和指导广告产业发展工作,分析了当前形势,部署了2022年重点任务,要求持续强化广告导向监管,着力规范和净化广告市场秩序。
《医疗美容广告执法指南》第五条指出,市场监管部门依法整治各类医疗美容广告乱象,着力解决危害性大、群众反映集中的问题,对部分情形予以重点打击,其中包括:宣传诊疗效果或者对诊疗的安全性、功效做保证性承诺,对食品、保健食品、消毒产品、化妆品宣传与医疗美容相关的疾病治疗功能等。
从此次部分医美器械调整内容来看,宏观描述产品的预期用途里,首次提到了“减轻皮肤皱纹,收缩毛孔,紧致、提升皮肤组织,保湿、补水……”等这些名词。品名举例也分别确定了“射频治疗仪、射频皮肤治疗仪、注射用透明质酸钠溶液、面部埋植线、面部提拉线、面部锥体提拉线”。
我们知道,医疗器械的产品描述和预期用途,是对一类产品共性内容的基本描述,用于指导具体产品所属类别的综合判定,列举的品名举例为符合《医疗器械通用名称命名规则》的规范性、代表性名称。
此次预期用途和品名举例的调整,明确各概念的定义及应包含的要素,有利于消费者了解预期用途是否与心理预期匹配,有益于在医疗器械监管中建立统一的认识,使监管工作更科学。
由此我们可以预判,调整后的医美器械将在生产、销售、使用、广告宣传上,迎来更全面更规范的相关行业大检查。我们期待,能够彻底清除扰乱行业秩序的黑医美,让喧嚣、纷乱归于宁静规范,还医美行业一片净土。(凌燕)
